Resumo sobre Ligações químicas - Química

LIGAÇÕES QUÍMICAS
Resumo elaborado por: @jalecodaval
Representações
- Fórmula eletrônica (Fórmula de Lewis)
- Fórmula estrutural
- Fórmula molecular
Objetivo
Attingir a estabilidade química dos gases nobres (Regra do octeto)
Tipos de Ligações
Iônica
Metais X Ametais
- Formação de íons;
- Atração de origem eletrostática;
- Doação de elétrons;
- Composto iônico.
Propriedades:
- Sólidos;
- PE e PF altos;
- Conduzem energia elétrica;
- Funções ao dissolverem em água.
Covalente
Ametais X Ametais
- Compartilhamento de elétrons;
- Composto molecular.
Tipos:
- POLAR (Elétrons diferentes)
- APOLAR (Elétrons iguais)
Ligações:
- NORMAL (1 elétron de cada átomo)
- DATIVA (1 par ou + de elétrons do mesmo átomo)
Metálica
Metais X Metais
- Elétrons livres nos metais;
- Mar de elétrons;
- Liga metálica.
Propriedades:
- Sólidos;
- Possuem brilho;
- Altas condutividades;
- PE e PF altos.
Conceitos Adicionais
Aloptropia
Quando um mesmo elemento forma substâncias diferentes. Exemplos principais: C, P, O, S.
Ligações Sigma (σ) e Pi (Ï€)
Sigma (σ): ligação simples
Pi (Ï€): ligação dupla ou tripla 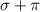 ou
ou 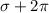
Estude agora:



