O sulfato, naturalmente presente em águas de chuva, pode ser determinado quantitativamente com base na reação entre o sulfato e o bário, representada pela equação química a seguir.
NaSO4(aq) + Ba(NO3)2(aq) → BaSO4(s) + NaNO3(aq)
Com base na equação, assinale a alternativa que apresenta o tipo de reação química envolvida na determinação de sulfato.
O átomo neutro de potássio (K) apresenta número de prótons e de massa iguais a 19 e 39, respectivamente. Ao perder um elétron, este átomo neutro se transforma em cátion, de carga elétrica +1.
Com base nessas informações e nos conhecimentos sobre estrutura de átomos, assinale a alternativa que apresenta, corretamente, o número de elétrons deste cátion formado.
Um elemento químico, representado por T, tem número atômico igual a 38.
Sobre o elemento T, e com base nos conhecimentos sobre a classificação periódica, assinale a alternativa correta.
Num laboratório de química havia dois frascos contendo soluções aquosas de ácido nítrico (HNO3). No primeiro frasco a solução tinha concentração de 0,2 mol L−1 e volume de 500 mL; no segundo, a solução tinha concentração de 0,8 mol L−1 e volume de 100 mL. Para evitar desperdício, o técnico desse laboratório resolveu misturar as soluções de ambos os frascos.
Em relação ao texto e ao conceito de concentração de solução, assinale a alternativa que apresenta, corretamente, o valor da concentração da solução de HNO3 resultante.
Considere o sistema a seguir, em equilíbrio, a uma temperatura de 80 °C:
C(s) + CO2(g) ⇌ 2CO(g)
Em relação ao sistema e supondo que as pressões parciais de equilíbrio de CO2 e CO sejam 3,0 e 6,0 atm respectivamente, considere as afirmativas a seguir. Dados: R = 0,082 atm L K−1 mol−1
I. A expressão para a constante de equilíbrio da reação, em termos de pressão (Kp), é 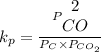
II. Nessa reação, os reagentes e produto formado constituem um sistema homogêneo.
III. Ao adicionar certa quantidade de CO2(g) ao sistema, ocorrerá um aumento na concentração de CO(g).
IV. O valor numérico da constante de equilíbrio para a reação, em termos de pressão (Kp), é 12 atm.
Assinale a alternativa correta.
Considere os seguintes pares de compostos.
I. metoximetano e etanol
II. metoxipropano e etoxietano
III. metilpropano e butano
Em relação a esses compostos e aos conceitos de isomeria, assinale a alternativa que apresenta, corretamente, o(s) par(es) que apresentam metameria.








