Considere a equação da transformação geral dos gases:
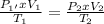
À temperatura de 300 K, uma amostra de gás hidrogênio ocupa um volume de 0,15 L à pressão de 0,5 atm.
O volume aproximado ocupado por essa amostra a 293 K em uma transformação isobárica é
Analise as informações de um produto químico.

A fórmula molecular e o estado físico a –156 ºC e a –35 ºC do produto químico mencionado são, respectivamente,
Considere o íon do elemento químico hipotético A:
![]()
As quantidades de prótons, nêutrons e elétrons do íon apresentado são, respectivamente,
O dióxido de enxofre (SO2) é um gás produzido pela combustão do enxofre. Sua oxidação produz o trióxido de enxofre (SO3), que, em contato com água, forma o ácido sulfúrico (H2SO4).
Com relação aos compostos e às estruturas moleculares mencionadas, pode-se afirmar que:
A reação de síntese mais utilizada para a formação do metanol (CH3 OH), um biocombustível muito utilizado nas indústrias químicas como solvente, ocorre a partir da reação entre os gases monóxido de carbono (CO) e hidrogênio (H2 ). A equação não balanceada que representa a reação é:
CO (g) + H2(g) → CH3OH (ℓ)
Em uma reação de síntese do metanol, com 100% de rendimento, foi empregado 25 g de hidrogênio gasoso e quantidade suficiente de monóxido de carbono.
A quantidade máxima de metanol produzida nessa síntese é igual a
Analise o equilíbrio químico que envolve a formação do gás cloreto de hidrogênio (HCℓ).
2Cℓ2 (g) + 2H2O (g) + 113 kJ ⇌ 4HCℓ (g) + O2 (g)
Considerando o equilíbrio químico mencionado, para aumentar o rendimento do gás cloreto de hidrogênio nesse sistema é preciso









