O esquema representa a teoria das colisões. Em condições adequadas, os reagentes colidem e formam o complexo ativado, que dá origem aos produtos.

A energia necessária para ocorrer a formação do complexo ativado é denominada . A energia dos produtos da reação é energia necessária para a formação do complexo ativado.
As lacunas do texto são reenchidas, respectivamente, por:
Em uma aula de química foram realizados cinco experimentos para o estudo da rapidez das reações a partir da mistura de volumes adequados dos seguintes reagentes: ácido oxálico (incolor) (C2H2O4), ácido sulfúrico (incolor) (H2SO4) e permanganato de potássio (violeta intenso) (KMnO4). A reação entre esses reagentes forma produtos incolores. Foi medido com cronômetro o tempo despendido para a cor violeta intenso desaparecer completamente.
O esquema desse experimento é representado na figura.

Na tabela constam os dados dos experimentos. Em todos eles foram usados os mesmos volumes dos reagentes.

Em um dos experimentos foi usado um catalisador.
Esse experimento é o de número
Uma reação química pode atingir um estado em que os processos direto e inverso ocorrem com a mesma velocidade (ou rapidez). Esse estado é o equilíbrio químico. A constante de equilíbrio é dada pela lei da ação das massas. Para a uma equação geral do equilíbrio representado por aA + bB
⇌ cC + dD a constante do equilíbrio, Kc, é dada por: 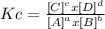
A concentração de um sólido, ou de um líquido puro, não varia independentemente de sua quantidade no processo. Analise o seguinte sistema em equilíbrio
%2BO_2(g)%5Crightleftharpoons2H_2O(l)%2B2C%20%5Cell_2(g))
Para esse sistema em equilíbrio, a constante de equilíbrio, Kc, é dada por:
A interação dos gases dióxido de enxofre (SO2) e oxigênio (O2) em um sistema fechado resulta na formação do gás trióxido de enxofre (SO3) em uma reação exotérmica, que é representada pelo equilíbrio reacional:
2SO2 (g) + O2 (g) ⇌ 2SO3 (g) ΔHo < 0
A condição que interfere deslocando o equilíbrio reacional no sentido da formação de SO3 é a
Na tabela são dadas as equações de reações de diversos compostos de crômio, em que esse elemento se apresenta em diversos estados de oxidação.

A reação em que ocorre processo de oxirredução é a
Considere o texto e os dados para responder à questão.
Na figura é apresentada uma pilha de Daniel, as reações que nela ocorrem e uma representação esquemática das alterações que ocorrem nas placas de seus eletrodos de cobre e de zinco.

O potencial da pilha (Eº pilha) pode ser previsto por meio da equação:
Eº pilha = Eº cátodo – Eº ânodo
Na tabela estão apresentados os potenciais padrão de redução de alguns metais.

Na pilha de Daniel, o tipo de reação que ocorre sobre a placa de cobre, o nome do componente X indicado na figura pela seta e a função desse componente são, respectivamente:









