Sobre as reações químicas, são feitas as seguintes afirmativas. Assinale V para as verdadeiras e F para as falsas.
I- nem toda colisão com orientação adequada produz uma reação, sendo necessário que a colisão entre os reagentes ocorra com uma energia igual ou maior que a energia de ativação da reação.
II - a energia mínima para uma colisão efetiva é denominada energia de ativação.
III - um aumento de temperatura significa um aumento de energia cinética das moléculas ou dos íons dos reagentes, o que provoca um aumento de colisões efetivas por unidade de tempo.
IV - para acelerar uma reação, é necessário aumentar a concentração dos reagentes, ou aumentar a pressão (se os reagentes estiverem na fase gasosa), ou ainda aumentar a temperatura.
V- para retardar uma reação muito rápida, deve-se diminuir a concentração dos reagentes, ou diminuir a pressão (se os reagentes estiverem na fase gasosa), ou ainda diminuir a temperatura.
A sequência de cima para baixo está correta em:
A efedrina é uma amina simpatomática similar aos derivados sintéticos da anfetamina, muito utilizada em medicamentos para emagrecer, pois ela faz com que o metabolismo acelere, queimando mais gordura (através da termogênese), porém causa uma forte dependência, o que fez a droga ser proibida para este uso, mas ainda hoje pode ser encontrada em algumas farmácias em forma de remédios destinados para problemas respiratórios, sendo indicada no tratamento das patologias do sistema respiratório como asma, bronquite, rinites, sinusite crônica, gripes, congestão nasal, cefaleias, enfisema e sudorífica.

A respeito da fórmula estrutural da efedrina, são feitas as seguintes afirmações:
I - sua fórmula molecular é C10H15NO.
II- as funções álcool e amida estão presentes.
III - a molécula apresenta um carbono quiral (assimétrico).
Das afirmações acima, são CORRETAS:
Substâncias com propriedades detergentes (sabões ou detergentes) são agentes tensoativos, isto é, possuem a capacidade de diminuir a tensão superficial da água e são constituídas por moléculas contendo uma parte orgânica (não polar), e um grupo iônico (polar), o que contribui para a remoção de partículas de gordura ou óleo presentes nos utensílios domésticos. Geralmente a maioria dos detergentes usados no Brasil são produzidos a partir da mistura de dodecanoato de sódio (I) ou alquil-benzeno-sulfonatos de sódio (II) e (III), de acordo com as estruturas apresentadas abaixo:
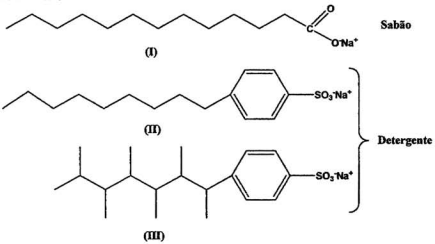
Com base nessas informações e nas estruturas (I), (II) e (III) apresentadas, são feitas as seguintes afirmações:
I - a parte hidrofóbica representada nas estruturas I, II e III associa-se às moléculas de água por ligações de hidrogênio.
II - a parte da molécula de sabão ou detergente que se fixa à gordura é de natureza apolar e a parte que se liga à molécula de água tem caráter polar.
III - os detergentes fabricados a partir de compostos com cadeia carbônica ramificada são biodegradáveis.
IV - diferentemente do detergente, o sabão é completamente decomposto por bactérias nas estações de tratamento, isto é, é 100% biodegradável.
Das afirmações acima, são CORRETAS:
A reação eletroquímica entre o zinco e cloro tem sido usada para gerar energia elétrica em baterias de carros.
Qual o rendimento teórico de cloreto de zinco, se uma amostra de 32,5 g de zinco reage com excesso de cloro? E se somente 61,0 g de cloreto de zinco são obtidos, qual o rendimento percentual?
O Índice que registra a quantidade de chuvas caídas no início da estação chuvosa no Ceará, em 2018, está abaixo da média histórica para o período. E com o intuito de medir o pH das águas das chuvas, alunos do curso de Química da UVA coletaram duas amostras em regiões distintas na Cidade de Sobral e as armazenaram em dois recipientes, de acordo com as seguintes especificações: Frasco (I), coletado na zona rural de Sobral, próximo ao distrito de Jaibaras; e Frasco (II) coletado no Sitio Santa Helena, próximo à fábrica de cimento.
Supondo que a água do Frasco (I) apresentou um pH=6,0, e sabendo que a água do Frasco (II) é 100 vezes mais ácida, qual o pH da água da chuva coletada próximo à fábrica de cimento?
A entalpia é uma propriedade extensiva. Desta forma, a magnitude do AH é diretamente proporcional à quantidade de reagente consumida no processo. Na combustão do metano, para formar dióxido de carbono e água líquida, por exemplo, são produzidos 890 kJ de calor, quando 1 mol de metano sofre combustão em um sistema à pressão constante, como mostra a equação química a seguir:
CH4(g) + 202(g) — CO2(g) + 2H2O(I) ΔH = -890 kJ
Qual a quantidade aproximada de calor é liberada quando 8,00 g de gás metano são queimados em um sistema à pressão constante?









