O diclorodifenilnitrocloroetano (DDT) é o mais conhecido entre os inseticidas do grupo dos organoclorados. Ele foi usado na Segunda Guerra Mundial, para prevenção do tifo em soldados, que o utilizavam na pele para combater os piolhos; posteriormente, seu uso passou a ser agropecuário. Esse tipo de inseticida atua sobre o sistema nervoso central, ocasionando distúrbios sensoriais e problemas relacionados à respiração. Segundo notícia veiculada na Revista Exame, 1 em cada 4 cidades está com sua água contaminada pelo DDT.
Disponível em: https://exame.abril.com.br/brasil/1-em-4-municipios-tem-coquetel-comagrotoxicos-na-agua-consulte-o-seu/. Acesso em: 19 set. 2019. (Adaptado).
Observe, a seguir, a figura da estrutura do DDT.

Sobre o DDT, é correto afirmar que
Ácidos e bases são substâncias presentes em inúmeros processos químicos que ocorrem ao nosso redor, desde processos industriais até processos biológicos e reações que ocorrem no ambiente. A força relativa desses ácidos ou bases podem ser expressas quantitativamente a partir de sua constante de equilíbrio ácida ou básica. Analise a tabela a seguir com alguns ácidos e bases ordenados em função de sua capacidade de doar ou receber prótons e seus respectivos valores de Ka e Kb.
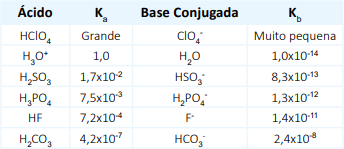
Com base na análise da tabela e nas propriedades dos ácidos e bases, assinale a alternativa correta.
A busca por materiais de alto valor agregado, alta aplicabilidade e sustentabilidade motiva inovações em todas as áreas da ciência. O carbeto de tungstênio (WC) é uma substância extremamente dura, composta por uma liga intersticial muito utilizada na fabricação de abrasivos, materiais muito duros que arrancam, por atrito, partículas de outros materiais. O carbeto de tungstênio é obtido a partir da seguinte reação química:
W(s) + C(s) → WC(s)
Com base nessa reação, ao calcular o valor de ΔHf usando a Lei de Hess e as seguintes reações de combustão, assinale a alternativa correta.
W(s) + 3/2O(g) → WO3(s) ΔHcomb = - 840 kJ/mol
C(s) + O2(g) → CO2(g) ΔHcomb = - 394 kJ/mol
WC(s) + 5/2O2(g)→WO3(s) + CO2(g) ΔHcomb = - 1196 kJ/mol
A mistura de água e álcool etílico não mantém a aditividade dos volumes. Esse fato pode ser observado de forma perceptível, quando se misturam 50% de água e 50% de álcool etílico.
Assinale a alternativa que explica corretamente esse fato.
Em uma aula experimental de Química no 1º ano do ensino médio, os estudantes, divididos em grupos, tentaram descobrir por que alguns materiais se misturam e outros não. Para isso, utilizaram reagentes de uso cotidiano: água, óleo de soja, vinagre, glicerina, sal de cozinha. O roteiro experimental utilizado está descrito na tabela a seguir.

De acordo com os resultados obtidos na aula experimental e os conhecimentos sobre ligações químicas, polaridade e forças intermoleculares, é correto afirmar que
Atualmente, o etanol (C2H5OH) é um dos principais combustíveis alternativos aos oriundos do petróleo. Uma de suas maiores vantagens é o fato de ele ser um combustível renovável e que o comercializado nos postos de combustível tem em média 96% de pureza.
(Densidade do etanol a 20° C: 0,810 g/cm3)
Considerando esse valor de pureza, é correto afirmar que a combustão completa de 1 litro de etanol









